Advantages
- FAP遺伝子強制発現がん細胞ではなく、生体内でマウス由来の間質が自然に形成される臨床近似モデルで、有効性を確認
Current Stage and Key Data
Current Stage:マウス移植腫瘍モデルでの治療効果(PoC)取得済み。
Future Plan:アスタチン以外の核種への展開検討中。FAPα親和性化合物を改良中。
Key Data
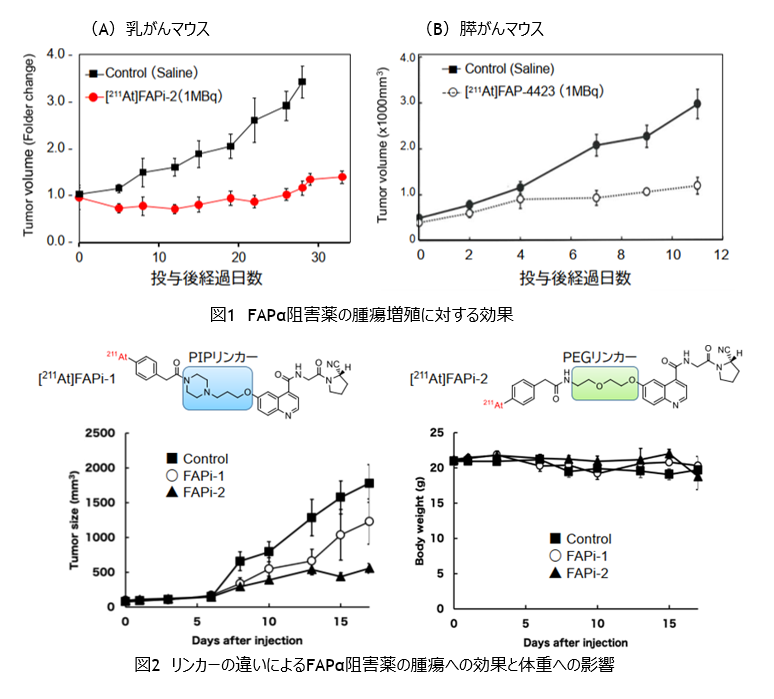
・ 乳がん移植マウスおよび膵がん移植マウスに対し、アスタチン標識FAPα阻害薬([211AT]FAPi-2、[211AT]FAP-4423)を投与したところ、どちらも腫瘍増殖を有意に抑制した(図1)。
・ リンカー構造の異なるFAPα阻害薬([211AT]FAPi-1 、[211AT]FAPi-2)を膵がん移植マウスに投与したところ、PEGリンカーを有する[211AT]FAPi-2がより腫瘍増殖を抑制した。また、体重へ影響は見られなかった(図2)。
Partnering Model
大阪大学では、本技術にご関心のある放射性医薬品・オンコロジー領域の製薬企業様・バイオテック企業様を探索しています。ご興味ございましたら、研究代表者との技術ディスカッションの面談をアレンジいたします。
Background and Technology
膵臓がんやトリプルネガティブ乳がんなどの難治性がんでは、腫瘍周囲が線維性間質で厚く覆われ、薬剤の浸透を阻害する「物理的バリア」として機能することが、治療抵抗性と予後不良の一因とされている。この間質を構成する腫瘍随伴線維芽細胞では、線維芽細胞活性化タンパク質α(FAPα)が特異的に高発現しており、FAPαを標的とした薬剤送達は、固形がん全般に応用可能な有望な戦略として世界的に開発が進められている。
本技術では、FAPαに高親和性を有するFAP阻害剤(FAPI)に対し、放射性核種を標識したコンジュゲートを開発した。FAP強制発現モデルではなく、生体内で自然な間質形成が生じる臨床像に近いマウスモデルでPoCを取得しており、実臨床での高い再現性が期待される。さらに、治療用核種と診断用核種を切り替えることで、同一化合物骨格を用いた画像診断と治療の一体的なセラノスティクス展開も可能となる。
Principal Investigator
白神 宜史 招へい准教授 (大阪大学 放射線科学基盤機構)
Patents and Publications
PCT/JP2023/006110